- ⌂
-
Le DPM
Les Equipements
L'Environnement
Zoom sur... Le Bâtiment André Rassat
Nommé d'après une figure tutélaire de la chimie grenobloise, ce bâtiment est recouvert d’une double peau en feuille métallique qui apporte une protection thermique sur 3 côtés et crée une unité architecturale favorisant l'intégration parmi les arbres du site.
-
Thématiques
Le Thème
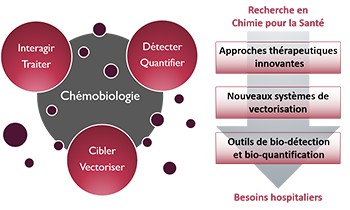
« Approches thérapeutiques innovantes »De nouvelles solutions thérapeutiques, de la cible biomacromolécu-laire émergente aux approches originales pour traiter les maladies
Le Thème
« Nouveaux systèmes de vectorisation »Combiner les propriétés d’inclusion de principes actifs, de franchisse-ment de barrières, d’adressage et de relar-gage en milieu vivant
Le Thème
« Outils de bio-détection et bio-quantification »Des dispositifs analytiques originaux pour la détection de cibles, de l’ion au micro-organisme en milieu complexe
Zoom sur... La Chémobiologie
-
Équipes
L'Équipe « COMET »
« COMET » développe la conception rationnelle, la synthèse et/ou l'extraction de composés à forte diversité/complexité comme nouveaux agents thérapeutiques et outils moléculaires pour la pénétration cellulaire ou la détection de biomolécules, actifs in vivo.L'Équipe « NOVA »
« NOVA » utilise des acides nucléiques fonctionnels comme éléments de reconnaissance pour des applications thérapeutiques ou diagnostiques, comme la sélection d'oligonucléotides, ou le développement de dispositifs d'analyses et de nanovecteurs.Les Services
-
Productions
Les Publications
La Vulgarisation
Les JSM
Zoom sur... La 12ème JSM (15 juin 2023)
Le DPM organise des journées scientifiques consacrées au médicament. L'objectif est de rassembler les spécialistes académiques et industriels autour d'une thématique. 2023 : Apports de la Chimie Click et de la Lumière en Chemobiologie
-
Partenariats
Les Formations
Les Consortiums
Les Financements
Zoom sur... L'environnement Grenoblois
Le DPM est un acteur central sur le bassin grenoblois en chimie, biologie et santé, lié au CHU Grenoble Alpes et à de nombreuses autres organisations : Pole de Recherche CBS, ICMG, Labex ARCANE, EUR CBH, Institut Carnot Polynat, Réseau GREEN.
Article
- Projet
- Ahcène BOUMENDJEL,
- Titre
- Recombinant tyrosinase from Polyporus arcularius: overproduction in Escherichia coli, characterization and use in a study of aurones as tyrosinase
- Auteurs
- E. Böhmová, M. Kotík, A. Křenková, P. Man, R. Haudecoeur, A. Boumendjel, R. Hardre, Y. Mekmouche, E. Courvoisier-Dezord, M. Réglier, L. Martínková
- Edition
- J. Agric. Food Chem. 64, 2925-2931.
- Année
- 2016
- Résumé
- The aims of this study were to examine the expression of a fungal tyrosinase gene in a prokaryotic host and to use the enzyme as a model of a eukaryotic tyrosinase. Specifically, the effects of various aurones (tyrosinase inhibitors, activators or substrates) on the enzyme were tested. The pro-tyrosinase from Polyporus arcularius was produced in Escherichia coli, partially purified in a Ni-affinity column and activated by trypsin-catalyzed removal of its C-terminal part. Trypsin cleaved the pro-tyrosinase after the R388 residue according to MALDI-TOF analysis of the active enzyme purified by size-exclusion chromatography. This enzyme was a homodimer and transformed L-DOPA (Km = 1.04 ± 0.08 mM, kcat = 223 ± 8 s-1), tert-butylcatechol, L-tyrosine, p-cresol, phenol and 4’- hydroxyaurones. 3’- and 2’-Hydroxyaurones acted as activators and 2’,4’-dihydroxyaurone as an inhibitor. The enzyme is a promising model for tyrosinase effector studies, being, in contrast to the commercial tyrosinase, a single isoenzyme.




 Annuaire
Annuaire Contact
Contact Plan d'accès
Plan d'accès ENG
ENG Login
Login